
DRA. MARTA VIVES-PI
Inmunología de la Diabetes
SERVICIO DE INMUNOLOGÍA
Unidad de Inmunología de la Diabetes. Instituto de Investigación Germans Trias i Pujol (IGTP), Badalona (BARCELONA)
AVANCES EN EL ÚLTIMO AÑO
Avances en el proyecto de la Dra. Marta Vives-Pi
Terapia contra la autoinmunidad para la prevención y la curación de la diabetes tipo 1. Nanopartículas tipo liposoma que re-educan el sistema inmunológico para permitir la regeneración de las células beta.
Actualizado: 01-12-2022
1. Introducción
El objetivo del grupo Inmunología de la Diabetes del Instituto de Investigación Germas Trias i Pujol (IGTP), es contribuir al desarrollo de una estrategia para corregir la autoinmunidad en la DMT1, re-educando el sistema inmunitario de forma definitiva mediante inmunoterapia y al mismo tiempo, avanzar en el conocimiento de la etiopatogenia de la enfermedad. El equipo investigador durante el último periodo (mayo 2021-diciembre 2022) ha estado formado por:
• Marta Vives-Pi, líder del grupo.
• David Perna-Barrull, investigador post-doctoral.
• Silvia Rodríguez-Fernández, investigadora post-doctoral
• Lidia Almenara, investigadora pre-doctoral.
• Rosa Ampudia, ténico en modelos experimentales.
• Laia Gómez-Muñoz, investigadora pre-doctoral.
• Marta Murillo, facultativa especialista en Pediatría.
• Aina Valls, facultativa especialista en Pediatría.
• Federico Vázquez, facultativo especialista en Endocrinología.
• Eva Aguilera, facultativa especialista en Endocrinología.
• Nati Real, diplomada en Enfermería.
2. Avances 2021-2022
Las nanopartículas diseñadas por nuestro grupo -llamadas liposomas- capaces de detener la autoinmunidad y prevenir la DMT1 experimental actúan re-educando el sistema inmunitario, mediante el efecto sobre unas células del sistema inmunitario llamadas dendríticas. El desarrollo preclínico de estas nanopartículas se lleva a cabo a través de la spin-off Ahead Therapeutics S.L (www.aheadtherapeutics.com) tal y como se presenta en el II Congreso Nacional DiabetesCERO (Granada, Marzo 2022) (apartado 2.1). Al mismo tiempo, seguimos trabajando para definir biomarcadores inmunológicos que nos permitan identificar el momento óptimo para administrar la inmunoterapia en un futuro (apartado 2.2) y en el estudio de los factores prenatales de susceptibilidad, concretamente el fármaco betametasona (apartado 2.3). Todos los estudios con muestras humanas y modelos experimentales han tenido la aprobación del Comité Ético del Hospital Germans Trias i Pujol de Badalona y del Comité Ético del CMCiB respectivamente.
Durante el último año la actividad del grupo ha dado como resultado 5 artículos científicos originales (publicados en revistas de alto factor de impacto), 8 comunicaciones a congresos científicos y más de 10 actividades de divulgación.
2.1 Estudio nº 1. Inmunoterapia para la DMT1. Esta línea prioritaria desarrolla una terapia innovadora basada en la modulación de la respuesta inmunitaria. Nuestro grupo ha diseñado unas nanopartículas (tipo liposoma) que re-educan el sistema inmunitario y detienen la destrucción de las células β. La inmunoterapia actúa como una vacuna, de manera específica, segura, definitiva y sin efectos secundarios. Tras demostrarse su efecto en el sistema inmunitario de ratones con DMT1 y en células del sistema inmunitario de pacientes con DMT1, en este último año se ha profundizado en su mecanismo de acción y se ha demostrado su versatilidad en otras enfermedades autoinmunitarias. Proyecto financiado por la Fundación DiabetesCERO (ver artículos) y a través de Ahead Therapeutics SL.
• Artículo en prensa (Nov 2022) en la revista Nanomedicine, Nanotechnology, Biology and Medicine:
Almenara-Fuentes L, Rodriguez-Fernandez S, Rosell-Mases E, Kachler K, You A, Salvado M, Andreev D, Steffen U, Bang H, Bozec A, Schett G, Le Panse R, Verdaguer J, Dalmases M, Rodriguez-Vidal S, Barneda-Zahonero B, Vives-Pi M. Inducing immune tolerance with liposomes encapsulating autoantigens. A platform for autoimmune diseases. Nanomedicine, nanotechnology, Biology and Medicine. In press, Nov 2022.
En este estudio se demuestra que la inmunoterapia con liposomas con péptidos de autoantígenos también detiene la autoinmunidad mediada por linfocitos T y por autoanticuerpos en modelos experimentales de otras enfermedades autoinmunitarias como la artritis reumatoide y la miastenia gravis. Estos estudios se han llevado a cabo en colaboración con la Universitat de Lleida, con el Institute of Myology de Paris (Francia) y con la Universidad de Erlangen (Alemania).
2.2. Estudio nº 2. Etapas de la enfermedad y biomarcadores. En esta línea, exploramos los mecanismos inmunológicos de la remisión parcial (luna de miel) al inicio de la DMT1, buscando marcadores de esta etapa (moléculas y células). Esta fase es de gran interés ya que reúne las condiciones de momento óptimo para administrar las futuras inmunoterapias. Proyecto financiado por el Instituto de Salud Carlos III co-financiado con fondos FEDER y la Fundación DiabetesCERO (ver artículos).
• Estudio publicado en la revista Frontiers in Immunology.
Gomez-Muñoz L, Gomez-Muñoz L, Perna-Barrull D, Caroz-Armayones JM, Murillo M, Rodriguez-Fernandez S, Valls A, Vazquez F, Perez J, Corripio R, Castaño L, Bel J, Vives-Pi M. Candidate biomarkers for the prediction and monitoring of partial remission in pediatric type 1 diabetes. Front Immunol 13:825426, 2022.
https://www. frontiersin.org/articles/10.3389/fimmu.2022.825426/full
En este estudio se han identificado biomarcadores y tipos celulares del sistema inmunitario de la etapa de remisión parcial. Los biomarcadores inmunológicos apoyan la participación de las defensas en la mejora metabólica de la luna de miel y sugieren intentos fisiológicos de frenar la autoinmunidad en esta fase. Las alteraciones observadas en la remisión parcial en ciertos tipos de leucocitos (linfocitos T reguladores, monocitos y células dendríticas), junto con la dosis total diaria de insulina son predictores de la luna de miel. Con estos datos hemos creado un modelo predictivo basado en un índice que incluye los porcentajes de estas células y que es capaz de predecir la aparición de la luna de miel justo en el momento del diagnóstico de la DMT1. Aunque estos datos son preliminares, estamos trabajando en la validaci.n de los biomarcadores y la mejora del algoritmo predictivo. Estos nuevos biomarcadores pueden ser útiles en la caracterización de la autoinmunidad en la remisión parcial, en la clasificación de los pacientes para futuros ensayos clínicos y en un control más personalizado de las personas con DMT1.
Este trabajo se ha llevado a cabo en colaboraci.n con el Hospital Universitari Parc Taul. de Sabadell, la Universidad Pompeu Fabra de Barcelona y el Instituto de Investigaci.n Sanitaria Cruces (Bilbao).
Seguimos trabajando para definir nuevas mol.culas que puedan ser biomarcadores y candidatas a nuevas estrategias terapéuticas.
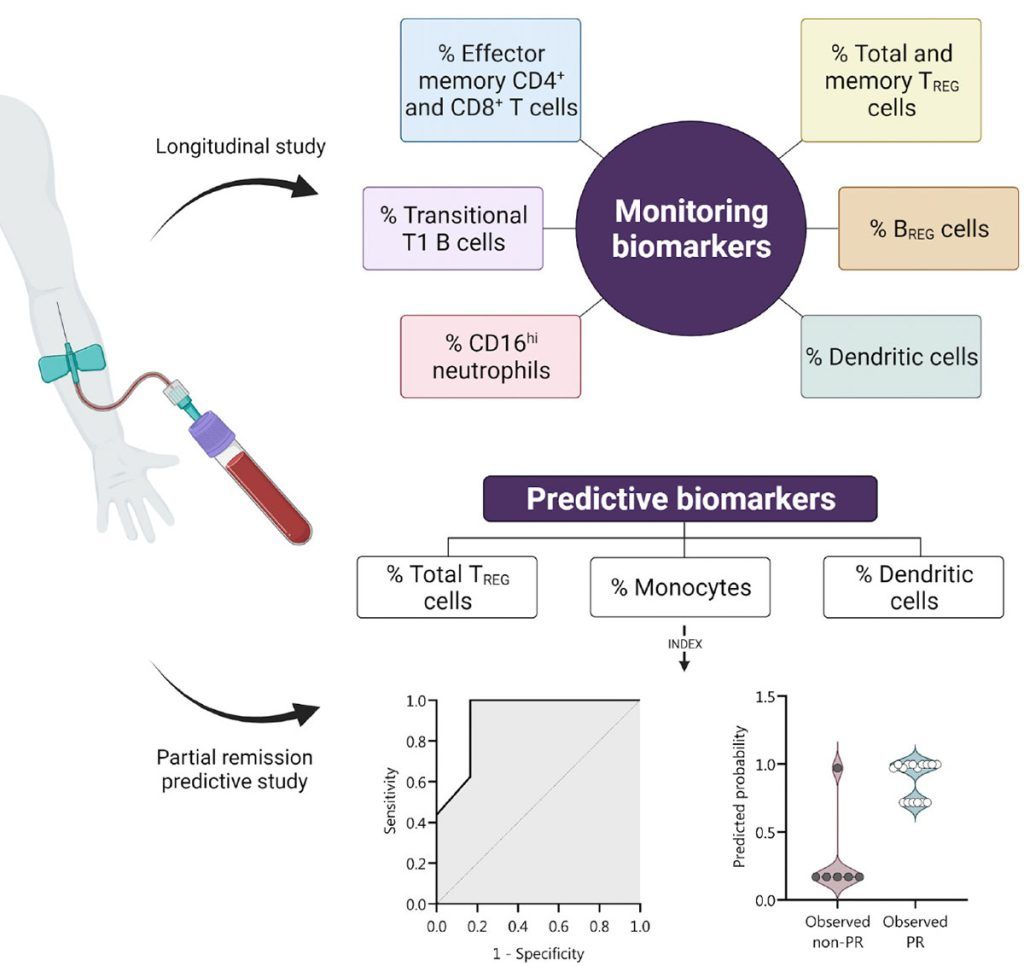
Figura 1. Alteraciones inmunológicas identificadas de la fase de remisión parcial (luna de miel) en sangre de pacientes pediátricos con DMT1 y su aplicación en un algoritmo predictivo. Los biomarcadores son principalmente células del sistema inmunitario (neutrófilos, células dendríticas y diversos subtipos de linfocitos. De: Gómez-Muñoz L (Figura no publicada a partir de datos de Front Immunol 13:825426, 2022)
Los biomarcadores pueden ayudarnos a identificar el momento óptimo para administrar una inmunoterapia en los ensayos clínicos y a estratificar los pacientes. Además, los biomarcadores específicos de las etapas de la DMT1 pueden tener un carácter predictivo. Por estas razones es necesario identificar más biomarcadores en la fase de luna de miel y otras etapas de la DMT1.
2.3. Estudio nº 3. Mecanismos patogénicos de autoinmunidad. Hasta la fecha se desconocen los desencadenantes ambientales de la autoinmunidad contra la c.lula beta. Esta línea de investigación se centra en una etapa especialmente sensible a estos factores: la etapa prenatal.
Nos interesa especialmente la maduración del sistema inmunitario en la etapa final del embarazo, y cómo ciertos fármacos a los que se expone la madre en esta fase modulan las defensas y por tanto la predisposición del bebé a desarrollar DMT1 y otras enfermedades autoinmunes. En este estudio nos hemos centrado en el efecto de la betametasona, un glucocorticoide que se administra a mujeres con riesgo de parto prematuro para mejorar la función pulmonar del bebé. Resultados previos de grupo demuestran que una sola dosis de este fármaco en la etapa prenatal modula el sistema inmunitario y la célula beta de ratones, protegiendo frente al desarrollo de la DMT1. Su efecto protector se ha estudiado en cohortes humanas mediante encuestas físicas y telemáticas a madres y padres de pacientes con DMT1 (Hospital Germans Trias i Pujol y de DiabetesCERO).
Proyecto financiado por la Fundación DiabetesCERO (ver artículos).
• Estudio publicado en la revista Jounal of Diabetes Research.
Perna-Barrull D, Murillo M, Real N, Gomez-Muñoz L, Rodriguez-Fernandez S, Bel J, Puig-Domingo M, Vives-Pi M. Prenatal betamethasone exposure and its impact on pediatric type 1 diabetes mellitus. A preliminary study in a Spanish cohort. Journal of Diabetes Research. ID 6598600, 2022.
https://doi.org/10.1155/2022/6598600
Las encuestas (más de 900 niños) indican que la exposición prenatal a la betametasona no incrementa el riesgo a desarrollar DMT1, e incluso sugieren un papel protector similar al observado en ratones. Esta línea de investigación se ha llevado a cabo en colaboración con la Fundación DiabetesCERO, la Universidad de Hamburgo y con la Unidad de Estadística y Bioinformática del Instituto de Investigación Vall d’Hebron (VHIR; Barcelona). Est. previsto explorar el posible papel de la betametasona en inmunoterapia combinada con los liposomas del apartado 2.1.
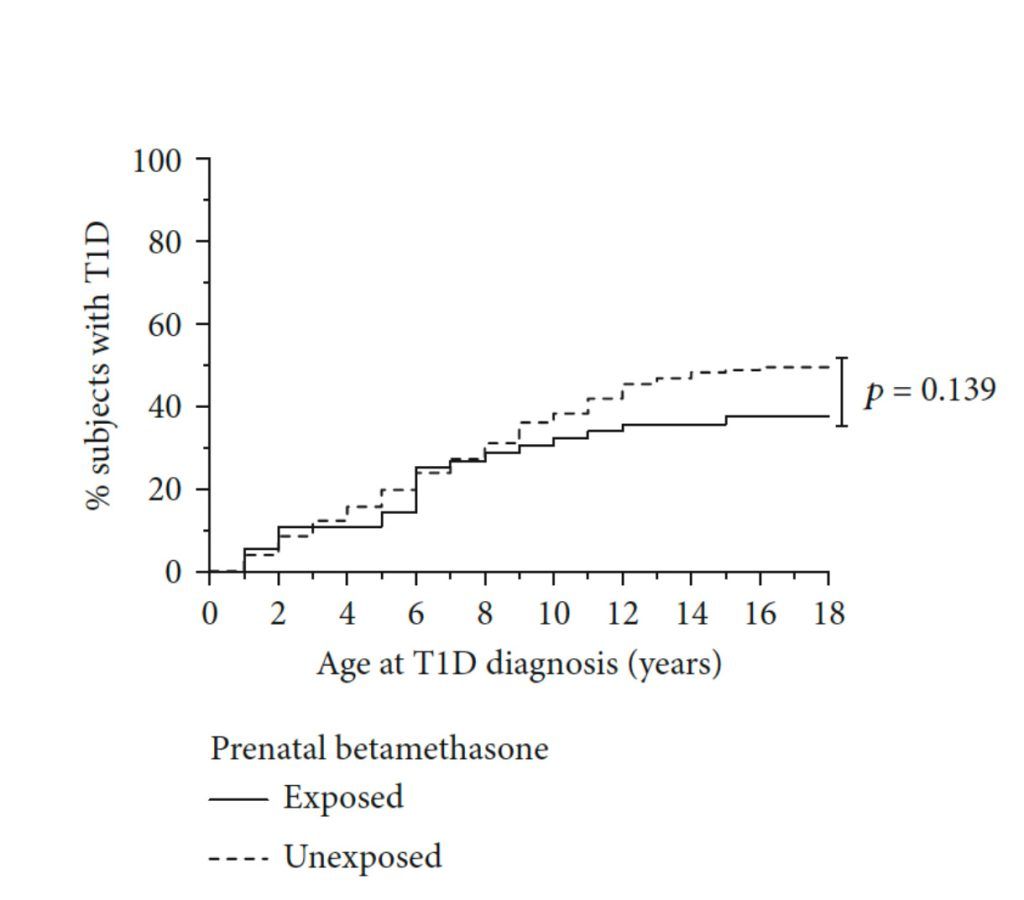
Figura 2.
La exposición prenatal a la betametasona tiende a reducir el porcentaje de personas con DMT1. En esta gráfica semuestra el porcentaje de niños que han desarrollado DMT1 dentro del grupo cuyas madres recibieron betametasona en la etapa final del embarazo (línea continua, n=56) en comparación con el grupo cuyas madres no recibieron el fármaco (línea discontinua, n=828). Se observa un menor porcentaje de niños con DMT1 en el grupo expuesto prenatalmente a la betametasona (37,5%) en comparación con el grupo no expuesto (49,52%). De: Perna-Barrull D et al, Journal of Diabetes Research 2022.
3. Conclusiones
En el último año hemos avanzado en el desarrollo de una inmunoterapia para la DMT1 y otras enfermedades autoinmunitarias, que corrige el defecto de tolerancia que causa la autoinmunidad de manera segura, con el objetivo principal de llegar a la pr.ctica cl.nica y que pueda ser combinada con estrategias de regeneraci.n de las c.lulas beta. En paralelo, hemos descrito nuevos marcadores inmunol.gicos de la etapa de remisi.n parcial en ni.os con DMT1 que han permitido crear una fórmula que predice en el momento del diagnóstico que personas van a desarrollar esta etapa. La importancia de esta predicción es poder definir la etapa óptima de administración de las futuras inmunoterapias. Al mismo tiempo, hemos identificado un factor ambiental -la exposición prenatal a la betametasona- que tiende a disminuir el riesgo a desarrollar la DMT1. Todo ello aumenta el conocimiento sobre la enfermedad y nos acerca a una terapia preventiva y terapéutica para la DMT1.
4. Publicaciones destacadas (2021-2022)
- Teniente-Serra A, Pizarro E, Quirant-Sánchez B, Fernández M, Vives-Pi M, Martínez-Cáceres EM. Identifying changes in peripheral lymphocyte subpopulations in adult onset type 1 diabetes. Front Immunol. 2021 Dec 6;12:784110. https://doi.org/10.3389/fimmu.2021.784110
- Gómez-Muñoz L, Perna-Barrull D, Caroz-Armayones JM, Murillo M, Rodriguez-Fernandez S, Valls A, Vazquez F, Perez J, Corripio R, Casta.o L, Bel J, Vives-Pi M. Candidate biomarkers for the prediction and monitoring of partial remission in pediatric type 1 diabetes. Front Immunol 13:825426, 2022. https://www.frontiersin.org/articles/10.3389/fimmu.2022.825426/full
- Perna-Barrull D, Murillo M, Real N, Gomez-Mu.oz L, Rodriguez-Fernandez S, Bel J, Puig-Domingo M, Vives-Pi M. Prenatal betamethasone exposure and its impact on pediatric type 1 diabetes mellitus. A preliminary study in a Spanish cohort. Journal of Diabetes Research, vol. 2022, Article ID 6598600, 8 pages, 2022. https://doi.org/10.1155/2022/6598600.
- Almenara-Fuentes L, Rodríguez-Fernández S, Rosell-Mases E, Kachler K, You A, Salvado M, Andreev D, Steffen U, Bang H, Bozec A, Schett G, Le Panse R, Verdaguer J, Dalmases M, Rodríguez-Vidal S, Barneda-Zahonero B, Vives-Pi M. Inducing immune tolerance with liposomes encapsulating autoantigens. A platform for autoimmune diseases. Nanomedicine, Nanotechnology, Biology and Medicine. En prensa, Diciembre 2022
- Perna-Barrull D, Gomez-Muñoz L, Rodríguez-Fernández S, Gieras A, Ampudia-Carrasco R, Almenara-Fuentes L, Risue.o RM, Querol S, Tolosa E, Vives-Pi M. Impact of betamethasone pretreatment on engrafment of cord blood derived hematopoietic stem cells. Archivum Immunologiae et Therapiae Experimentalis. En prensa, Diciembre 2022.
5. Colaboraciones
Se mantienen las colaboraciones científicas con grupos punteros en el área, destacando la Hamburg Universität (Hamburgo, Alemania), la Nara University (Nara, Japón), el CABIMER (Sevilla), el Diabetes Research Institute (Miami, USA), la Katholieke Universiteit Leuven (Leuven, Belgium), entre otras.
6. Más información

Grupo Inmunología de la Diabetes del Instituto de Investigación Germas Trias i Pujol (IGTP). Badalona, 1 de diciembre de 2022.

Dra. Marta Vives
IGTP
Nanopartículas tipo liposoma que reeducan el sistema inmunológico para permitir la regeneración de las células beta.
LOS OTROS
PROYECTOS DE INVESTIGACIÓN
QUE FINANCIAMOS

Dra. Rosa Gasa
IDIBAPS
Generación de células productoras de insulina a partir de células de la piel. Diseño de un armazón y mejora de la revascularización mediante inhibición de PTP1B.
¡Conoce las últimas novedades!

Dr. Benoit Gauthier
CABIMER
Activación de LRH1 mediada por BL001 para promover la transdiferenciación de células alfa a células beta en un modelo de diabetes autoinmune.
¡Conoce las últimas novedades!
Yo también investigo...
¿y tú?
Juntos podremos encontrar una cura para la diabetes tipo 1.




